Mục lục
DỊCH TỄ
Ung thư phổi được chẩn đoán vào khoảng 116,470 đàn ông và 109,690 phụ nữ ở Mỹ năm 2012, và 86% bệnh nhân chết trong vòng 5 năm. Ung thư phổi, nguyên nhân hàng đầu chết vì ung thư, chiếm khoảng 28% cái chết vì ung thư ở đàn ông và 26% ở phụ nữ. Đỉnh tỷ lệ mới mắc vào giữa 55 tới 65 tuổi. Tỷ lệ mới mắc giảm ở đàn oogn và tăng ở phụ nữ.
PHÂN LOẠI MÔ HỌC
Bốn dạng chính chiếm 88% ung thư phổi nguyên phát: dạng biểu bì (tế bào vảy), 29%; dạng tuyến (bao gồm phế quản-phế nang),35%; tế bào lớn, 9% và tế bào nhỏ (hay tế bào yến mạch),18%. Mô học (loại tế bào nhỏ cùng tế bào không nhỏ) là quyết định chính trong việc tiếp cận điều trị. Tế bào nhỏ thường biểu hiện lan rộng, trong khi không tế bào nhỏ thường khu trú.
Dạng biểu bì và tế bào nhỏ biểu hiện điển hình là những khối trung tâm, trong khi dạng tuyến và tế bào lớn biểu hiện nốt hay khối ngoại biên. Dạng tuyến và tế bào lớn chiếm 20-30% bệnh nhân.
NGUYÊN NHÂN
Nguyên nhân chính của ung thư phổi là việc hút thuốc lá. Tế bào ung thư phổi có ≥10 tổn thương gene mắc phải, chủ yếu đột biến ở gene ung thư ras; khuếch đại, tái sắp xếp, hay hay hoạt động phiên mã của họ gene ung thư myc; biểu hiện quá mức của bcl-2, Her2/neu, và telomerase; và mất đoạn NST 1p, 1q, 3p12-13, 3p14 (vùng gene FHIT), 3p21, 3p24-25, 3q, 5q, 9p (p16 và p15 chất ức chế kinase phụ thuộc cyclin), 11p13, 11p15, 13 q 14 (rb gene), 16q, và 17p13 (p53 gene). Mất 3p và 9p là sự kiện sớm nhất, được phát hiện trong tăng sản biểu mô phế quản; bất thường p53 và đột biến điểm ras thường chỉ tìm thấy trong những ung thư xâm lấn. Nhóm nhỏ hay đầy ý nghĩa những bệnh nhân ưng thư dạng tuyến có đột biến hoạt hoá ở gene thụ thẻ EGF, hay kích hoạt các sự kiên liên quan đến gen alk hay ros.
BIỂU HIỆN LÂM SÀNG
Chỉ 5-15% được phát hiện khi không có triệu chứng. Khối u trung tâm nội phế quản gây ho, ho ra máu, khò khè, khó thở, viêm phổ. Tổn thương ngoại biên gây đau, ho, khó thở, triệu chứng của áp xe phổi bắt nguồn từ khối chiếm chỗ. Di căn lan rộng của ung thư phổi nguyên phát có thể gây tắc khí quản, nuốt khó, khàn giọng, hội chứng Horner. Những vấn đề khác của di căn bao gồm hội chứng tĩnh mạch chủ trên, tràn dịch màng phổi, suy hô hấp. Di căn ngoài lồng ngực ảnh hưởng đến 50% bệnh nhân dạng biểu mô, 80% dạng tuyến và tế bào lớn, và >95% tế bào nhỏ. Những vấn đề lâm sàng do di căn não, gãy xương bệnh lý, xâm lấn gan, và chèn ép cột sống. Hội chứng cận ung có thể được biểu hiện những dấu chứng của ung thư phổi hay triệu chứng đầu tiên của tái phát. Triệu chứng hệ thống xuất hiện trong 30% và bao gồm sụt cân, không ngon miệng, sốt. Hội chứng nội tiế xuất hiện trong 12% và bao gồm tăng calci máu (dạng biểu bì), hội chứng tiết hormone lợi niệu không thích hợp (tế bào nhỏ), nữ hoá tuyến vú (tế bào lớn). Hội chứng mô liên kết cơ xương bao gồm ngón tay vùi trống trong 30% (chủ yếu là không tế bào nhỏ) và bệnh phình trướng xương khớp trong 1-10% (chủ yếu là dạng tuyến), vơi ngón tay vùi trống, đau, và sưng.
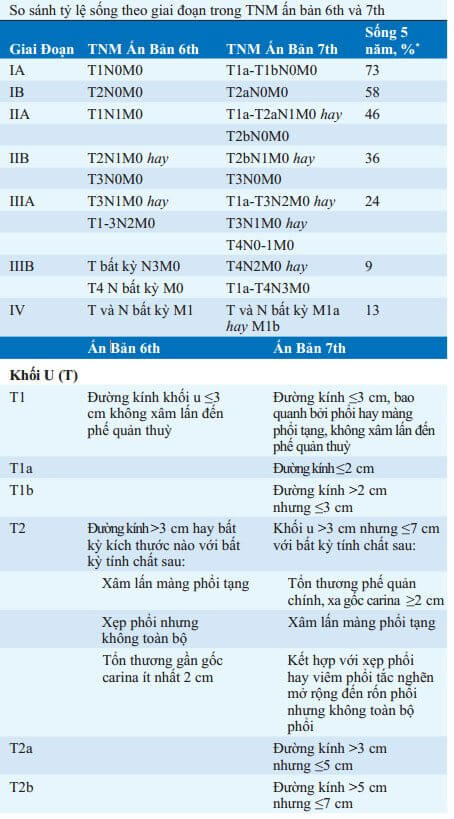
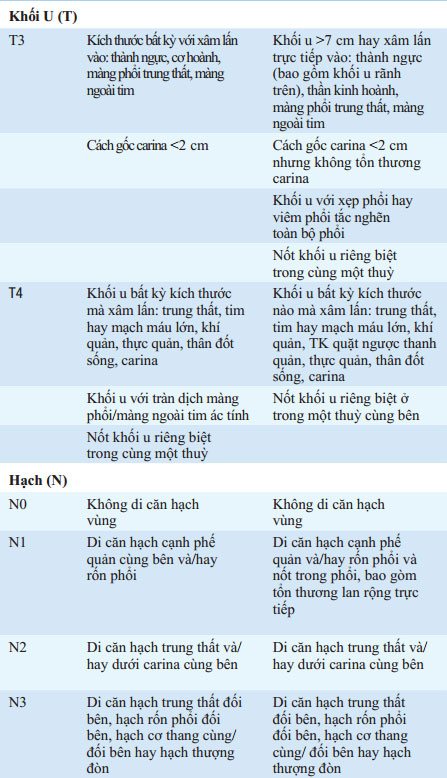
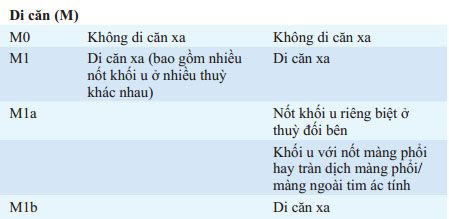
GIAI ĐOẠN (XEM BẢNG 76-1)
Hai phần để phân loại là (1) xác định vị trí (phân loại giải phẫu) và (2) đánh giá khả năng bệnh nhân chịu đựng điều trị kháng u (phân loại sinh lý). Khối u không tế bào nhỏ được phân loại theo TNM/Hệ thống phân loại quốc tế. T (khối u), N (hạch), và M (có di căn không?) để xác định những nhóm giai đoạn khác nhau. Khối u tế bào nhỏ được phân loại theo hệ thống hai giai đoạn: giai đoạn bệnh giới hạn – giới hạn một bên ngực và hạch lympho vùng; bệnh mở rộng – vượt giới hạn này. Thủ thuật phân loại chung bao gồm kháng cẩn thận tai, mũi và họng; X quang ngực, CT ngực bụng; và chụp cắt lớp positron. CT scan có thể gợi ý tổn thương hạch lympho trung thất và mở rộng màng phổi trong ung thư phổi không tế bào nhỏ, nhưng đánh giá xác định của di căn trung thất lan rộng yêu cầu xét nghiệm mô học. Quét hạt nhân phóng xạ thường quy không thực hiện ở bệnh nhân không triệu chứng. Nếu tổn thương khối trên CXR và không chống chỉ định rõ ràng cho điều trị phẫu thuật được ghi nhận, trung thất nên được kiểm tra. Những chống chỉ định chính cho điều trị phẫu thuật bao gồm di căn ngoài trung thất, hội chứng tĩnh mạch chủ trên, liệt dây thanh âm và thần kinh hoành, tràn dịch màng phổi ác tính, di căn phổi đối diện, và chẩn đoán mô học là ung thư tế bào nhỏ.
ĐIỀU TRỊ Ung Thư Phổi (Xem Bảng 76-2)
- Phẫu thuật cho bệnh nhân bệnh khu trú hay ung thư tế bào không nhỏ; tuy nhiên, đa số suy nghĩ ban đầu để điều trị cắt bỏ là cuối cùng chống lại bệnh di căn. Hoá trị hỗ trợ [cisplatin, 4 chu kỳ với 10mg/m2 cộng với thuốc hoạt hoá thứ hai (etoposide, vinblastine, vinorelbine, vindesine, taxane)] ở bệnh nhân cắt bỏ hoàn toàn trong giai đoạn IIA và IIB có thể kéo dài thời gian sống.
- Nốt phổi đơn độc: yếu tố gợi ý cắt bỏ gồm hút thuốc, tuổi ≥35, tỏn thương tương đối lớn (>2 cm), không calci hoá, triệu chứng ngực, và sự phát triển của tổn thương trên X quang. Xem Hình 76-1.
- Với ung thư phổi không tế bào nhỏ giai đoạn II không cắt bỏ, kết hợp xạ trị ngực và hoá trị với cisplatin làm giảm tỷ lệ tử vong khoảng 25 % vào năm đầu.
- Với ung thư tế bào không nhỏ không cắt, di căn, hay từ chối phẫu thuât: xem xét xạ trị; phối hợp với hoá trị cisplatin/taxane có thể giảm tỷ lệ tử vong khoảng 13% trong 2 năm và cải thiện chất lượng sống. Pemetrexed có tác dụng ở bệnh nhân bệnh tiến triển.
- Ung thư tế bào nhỏ: kết hợp hoá trị là phương thức điều trị căn bản; đáp ứng sau 6-12 tháng dự đoán thời gian sống còn trung bình và lâu dài.
- Xạ trị kết hợp với hoá trị trong ung thư phổi tế bào nhỏ giai đoạn giới hạn có thể tỷ lệ sống 5 năm từ 11% lên 20%.
- Chiếu xạ sọ não dự phòng cải thiện thời gian sống của ung thư phổi tế bào nhỏ giai đoạn giới hạn thêm 5%.
- Chiếu laser khối u thông qua nội soi phế quan thực hiện trong tắc nghẽn phế quản.
- Xạ trị với di căn não, chèn ép cột sống, khối có triệu chứng, và tổn thương xương.
- Khuyến khích ngừng hút thuốc.
- Bệnh nhân carcinom dạng tuyến (3% trong tất cả bệnh nhân ung thư phổi): 7% có đột biến hoạt hoá ở thụ thể yếu tố tăng trưởng biểu bì (EGF). Nhưng bệnh nhân này thường đáp ứng với gefitinib hay erlotinib, chất ức chế thụ thể EGF. Khoảng 5% bệnh nhân có hoạt hoá tái sắp xếp gene alk và có thể đáp ứng với crizotinib.
BẢNG 76-2 TÓM TẮT ĐIỀU TRỊ CHO BỆNH NHÂN UNG THƯ PHỔI
Ung Thư Phổi Tế Bào Không Nhỏ
Giai đoạn IA, IB, IIA, IIB, và đôi khi IIIA:
Phẫu thuật cắt bỏ với giai đoạn IA, IB, IIA, và IIB
Phẫu thuật cắt bỏ với nạo hạch trung thất hoàn toàn và xem xét CRx bổ trợ cho giai đoạn IIIA với “tổn thương N2 tối thiểu” (phát hiện lúc mở ngực hay mở trung thất)
Xem xét RT hậu phẫu cho bệnh nhân N2
Giai đoạn IB: thảo luận nguy cơ/lợi ích của CRx bổ trợ; không thực hiện thường quy
Giai đoạn II: CRx bổ trợ
RT tiềm năng cứu chữa cho bệnh nhân “không thể mổ”
Giai đoạn IIIA với các loại lựa chọn của khối u:
Khối u xâm lấn thành ngực (T3): cắt bỏ khối u cùng với tổn thương thành ngực và xem xét RT hậu phẫu
Khối u rãnh trên (Pancoast’s): RT hậu phẫu (30–45 Gy) và CRx kèm theo cắt bỏ phổi tổn thương và thành ngực với RT hậu phẫu.
Tổn thương đường dẫn khí gần (<2 cm từ gốc carina) không hạch trung thất: cắt nối khí quản hay phế quản nếu có thể bảo toàn phổi lành hay cắt toàn bộ phổi.
Giai đoạn IIIA “tiến triển, lâm sàng rõ ràng N2” (phát hiện trước phẫu thuật) và giai đoạn IIIB mà có thể dung nạp RT:
Tiềm năng cứu chữa đồng thời RT + CRx nếu tình trạng sức khoẻ hợp lý; ngược lại tuần tự CRx tiếp theo RT hay RT đơn lẻ.
Giai đoạn IIIB với xâm lấn carina (T4) nhưng không tổn thương N2:
Cân nhắc cắt toàn bộ phổi với cắt nối khí quản trực tiếp thông nối với phế quản chính đối bên.
Giai đoạn IV và giai đoạn IIIB tiến triển nhiều hơn:
RT vị trị có triệu chứng
CRx với bệnh nhân ngoại trú; xem xét CRx và bevacizumab
Dẫn lưu ngực với tràn dịch màng phổi ác tính lớn
Xem xét cắt khối u nguyên phát và di căn não hay tuyến thượng thận đơn độc.
Ung Thư Phổi Tế Bào Nhỏ
Giai đoạn giới hạn (tình trạng hoạt động tốt): kết hợp CRx + đồng thời RT ngực.
Giai đoạn mở rộng ( tình trạng hoạt động tốt): kết hợp CRx
Phản ứng khối u hoàn toàn (tất cả giai đoạn): RT dự phòng sọ não
Tình trạng hoạt động kém (tất cả giai đoạn):
Liều thay đổi kết hợp với CRx
Xạ trị giảm nhẹ
Phế quản phế nang hay carcinom tuyến với đột biến thụ thể EGF hay tái sắp xếp ALK
Gefitinib hay erlotinib, chất ức chế hoạt động kinase của thụ thể EGF
Crizotinib, chất ức chế alk
Tất Cả Bệnh Nhân
RT di căn não, chèn ép cột sống, tổn thương huỷ xương, triệu chứng tổn
thương khu trú (liệt thần kinh, tắc nghẽn đường dẫn khí, ho ra máu, tắc
nghẽn tĩnh mạch lớn trong lòng ngực, trong ung thư phổi không tế bào
nhỏ và ung thư tế bào nhỏ không đáp ứng với CRx)
Chẩn đoán thích hợp và điều trị các vấn đề y tế khác và chăm
sóc hỗ trợ trong suốt CRx
Khuyến khích ngưng hút thuốc
Tham gia các thử nghiệm lâm sàng, nếu đủ điều kiện
Viết tắt: CRx, hoá trị; EGF, yếu tố tăng trưởng biểu mô; RT, xạ trị. 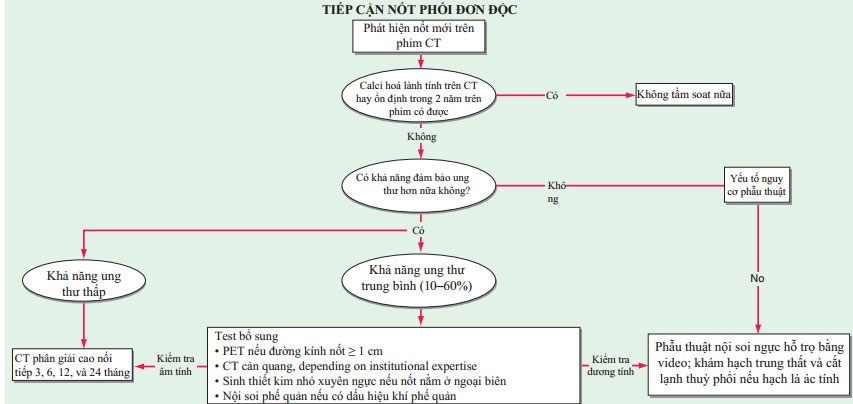
TIÊN LƯỢNG
Vào lúc chẩn đoán, chỉ 20% bệnh nhân có bệnh khu trú. Tỷ lệ sống trên 5 năm là 30% với đàn ông và 50% với phụ nữ có bệnh khu trú và 5% với bệnh nhân bệnh tiến triển.
TẦM SOÁT
Nghiên cứu của Viện Ung Thư Quốc Gia về tầm soát ung thư phổi ở người nguy cơ cao (tuổi từ 55 tới 74 có tiền căn hút 30+ gói-năm) với CT scan có hiệu ứng nhỏ trên tử vong chung.
