BƯỚU CỔ ĐA NHÂN ĐỘC (MNG)
Ngoài các đặc điểm của bướu cổ, biểu hiện lâm sàng của bướu cổ đa nhân độc bao gồm cường giáp dưới lâm sàng hoặc nhiễm độc giáp nhẹ. Các bệnh nhân thường là người già và có thể có biểu hiện rung nhĩ hoặc đánh trống ngực, nhịp tim nhanh, hồi hộp, run rẩy, hoặc giảm cân. Tiếp xúc gần đây với iod, từ thuốc cản quang hoặc các nguồn khác, có thể thúc đẩy hoặc làm trầm trọng thêm nhiễm độc giáp; điều này có thể phòng bằng cách kiểm soát trước các thuốc kháng giáp. Nồng độ TSH thấp. T4 có thể bình thường hoặc tăng rất ít; T3 thường cao hơn T4. Xạ hình tuyến giáp cho thấy sự hấp thụ không đồng nhất với nhiều vùng tăng và giảm; hấp thu iod phóng xạ 24h có thể không tăng. Nhân lạnh trong bướu cổ đa nhân nên được đánh giá theo cùng cách như nhân đơn độc (xem dưới đây). Thuốc kháng giáp, thường kết hợp với các thuốc chẹn beta, có thể bình thường hóa chức năng tuyến giáp và cải thiện triệu chứng nhiễm độc giáp trên lâm sàng nhưng không thuyên giảm. Thử nghiệm iod phóng xạ nên được xem xét ở mỗi bệnh nhân, nhiều người trong số họ là người già, để phẫu thuật. Cắt gần hết tuyến giáp giúp điều trị dứt khoát bệnh bướu cổ và nhiễm độc giáp. Những bệnh nhân điều trị thuốc kháng giáp chức năng tuyến giáp phải trở về bình thường trước khi can thiệp phẫu thuật.
U TUYẾN ĐỘC
Nhân tuyến giáp hoạt động tự trị, đơn độc là một u tuyến độc. Hầu hết các trường hợp do đột biến hoạt hóa tế bào soma của thụ thể TSH. Nhiễm độc giáp thường nhẹ. Xạ hình tuyến giáp để chẩn đoán xác định, cho thấy sự tập trung cục bộ ở nhân quá hoạt động và giảm tập trung ở phần còn lại của tuyến, như là khi hoạt động bình thường của tuyến giáp bị ức chế. Dùng iod phóng xạ với liều tương đối lớn (vd, 10-29,9 mCi 131I) thường là lựa chọn điều trị.
U TUYẾN GIÁP HYROID NEOPLASMS
Nguyên Nhân
U tuyến giáp có thể là lành tính (u tuyến) hoặc ác tính (ung thư). Ung thư biểu mô tuyến giáp bao gồm ung thư tuyến giáp thể nhú, thể nang và không biệt hóa. Tỷ lệ mắc bệnh ung thư tuyến giáp là ~ 9/100.000 mỗi năm.
Ung thư tuyến giáp thể nhú là loại phổ biến nhất của ung thư tuyến giáp (70-90%). Nó có xu hướng hình thành nhiều ổ và xâm lấn tại chỗ. Ung thư tuyến giáp thể nang là khó chẩn đoán thông qua hút bằng kim nhỏ (FNA) bởi vì sự phân biệt giữa u nang lành tính và ác tính chủ yếu dựa vào bằng chứng của xâm lấn mạch máu, dây thần kinh, hoặc cấu trúc lân cận. Nó có xu hướng lan tràn theo đường máu, di căn đến xương, phổi, và thần kinh trung ương. Ung thư biểu mô không biệt hoá là rất hiếm, ác tính cao và tử vong rất nhanh. U lympho tuyến giáp thường phát sinh trên nền của viêm tuyến giáp Hashimoto và xảy ra khi khối u tuyến giáp to nhanh. Ung thư biểu mô tuyến giáp thể tuỷ phát sinh từ các tế bào cận nang (C) sản xuất calcitonin và có thể xuất hiện không thường xuyên hoặc như là một rối loạn có tính chất gia đình, đôi khi kết hợp với đa u tuyến nội tiết type 2.
Đặc Điểm Lâm Sàng
Đặc điểm lâm sàng gợi ý ung thư biểu mô bao gồm thấy nhân hoặc khối gần đây hoặc tăng trưởng nhanh, tiền sử chiếu xạ vùng cổ, xuất hiện hạch bạch huyết, khàn tiếng, và cố định với mô xung quanh. Tăng kích thước tuyến nội tiết có thể dẫn đến chèn ép và chiếm chỗ của khí quản hoặc thực quản và triệu chứng tắc nghẽn. Tuổi <20 hoặc > 45, giới tính nam, và kích thước nhân giáp lớn thì tiên lượng xấu hơn.
Chẩn Đoán
Hướng tiếp cận đánh giá nhân đơn độc được mô tả ở Hình. 181-4
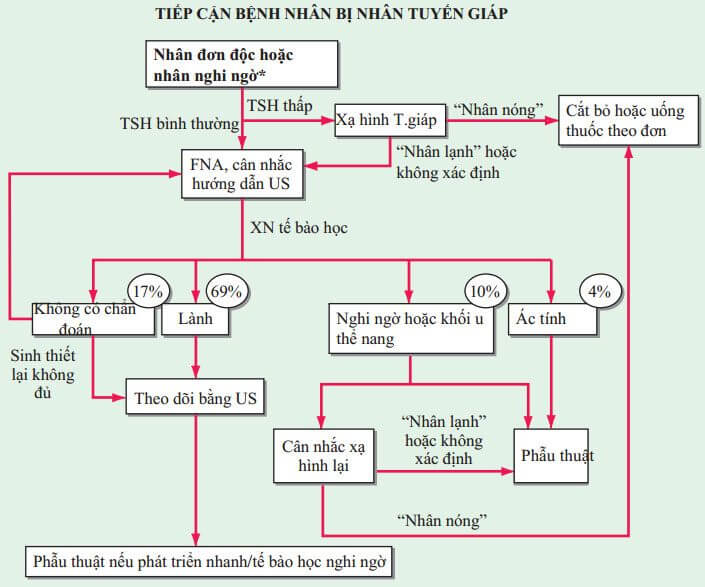
HÌNH 181-4 Tiếp cận bệnh nhân bị nhân tuyến giáp. *Khoảng 1/3 nhân tuyến giáp là nang hoặc hỗn hợp nang đặc. FNA, chọc hút bằng kim nhỏ; TSH, hormon kích thích tuyến giáp; US, siêu âm.
ĐIỀU TRỊ U Tuyến Giáp
Các nhân lành tính nên được theo dõi kiểm tra định kì. Ức chế TSH và dùng levothyroxin thì kích thước nhân giảm ở khoảng 30% bệnh nhân.
Điều trị ức chế TSH không vượt quá 6-12 tháng nếu không thành công. U tuyến thể nang không phân biệt được với ung thư biểu mô thể nang trên phân tích tế bào học mẫu hút bằng kim nhỏ. Cắt tuyến giáp (cắt thuỳ hay gần hết tuyến giáp) cần được hội chẩn trước khi phẫu thuật. Cắt gần hết tuyến giáp là cần thiết ở ung thư biểu mô thể nhú và thể nang và cần được thực hiện bởi bác sĩ có nhiều kinh nghiệm trong phẫu thuật này. Nếu các yếu tố nguy cơ và đặc trưng bệnh lí cho thấy cần phải điều trị iod phóng xạ, bệnh nhân cần được điều trị
trong vài tuần sau mổ với liothyronine (T3, 25μg 2-3 lần/ngày), tiếp theo ngừng điều trị thuốc thêm 2 tuần để phá hủy các mô còn sót lại sau phẫu thuật bằng sóng cao tần. Liều điều trị 131I được kiểm soát đến khi nồng độ TSH >50 IU/L. Ngoài ra, TSH tái tổ hợp có thể được sử dụng để nâng cao nồng độ TSH bị phá hủy trước đó. Điều này dường như là có hiệu quả tương đương với ngừng hormone tuyến giáp để điều trị phá hủy bằng sóng cao tần. Tiếp theo dùng levothyroxin ức chế TSH xuống thấp, nhưng có thể phát hiện được, ở nồng độ (0,1-0,5 IU/L) nên cố gắng ở những bệnh nhân có nguy cơ tái phát thấp, và đến một nồng độ bị ức chế hoàn toàn ở những người có nguy cơ tái phát cao. Trong trường hợp nguy cơ tái phát cao, T4 tự do nên được theo dõi để tránh quá liều. Theo dõi xạ hình và thyroglobulin huyết thanh (hoạt động như chỉ điểm u ở bệnh nhân không có hoặc rối loạn hoàn toàn chức năng tuyến giáp) nên được thực hiện đều đặn sau khi ngừng điều trị hormon tuyến giáp hoặc dùng TSH tái tổ hợp của người.
Phẫu thuật để kiểm soát ung thư biểu mô tuyến giáp thể tuỷ, vì những khối u này không hấp thụ iod phóng xạ. Xét nghiệm đột biến RET nên được thực hiện để đánh giá MEN-2 kèm theo, và sàng lọc trong gia đình nếu xét nghiệm dương tính. Sau phẫu thuật, calcitonin huyết thanh là dấu hiệu của bệnh tái phát hoặc còn sót mô ung thư.
