Có 3 bước chủ yếu giúp virus HIV xâm nhập vào tế bào T – CD4:
- HIV gắn vào recceptor của tế bào CD4 nhờ protein vỏ gp120 (đích của các thuốc ức chế gắn kết),
- Gắn vào các đồng thụ thể (đích tác động của các thuốc đối kháng đồng thụ thể) thông qua thay đổi cấu hình và cuối cùng là
- Hợp nhất virus và tế bào (đích tác động của thuốc ức chế hòa màng).
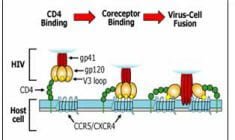
Hình 1: Ba bước chính của quá trình HIV xâm nhập vào trong tế bào (lấy từ: Moore JP, Doms RW. The entry of entry inhibitors: a fusion of science and medicine. PNAS 2003, 100:10598-602).
Mặc dù rất khác biệt nhưng các thuốc ức chế virus gắn kết, thuốc ức chế coreceptor và thuốc ức chế hợp nhất virus với tế bào (“ức chế hòa màng”) vẫn hợp lại thành một nhóm thuốc chung là nhóm thuốc ức chế virus xâm nhập. Các thuốc ức chế virus xâm nhập vẫ mở ra một triển vọng hoàn toàn mới trong điều trị HIV trong những năm sắp tới. Mặt dù vậy, rất nhiều dữ liệu hiện nay vẫn chưa đi qua được giới hạn của khoa học cơ bản, và nhiều loại thuốc được bàn tới dưới đây có thể cuối cùng sẽ không xuất hiện, và trên thực tế đã có những thuốc chịu số phận như vậy.
Thuốc ức chế virus gắn kết
Việc gắn kết giữa CD4 và gp120 là bước đầu tiên của quá trình virus xâm nhập. Về lý thuyết thì sự gắn kết (tương tác) giữa CD4 và gp120 có thể bị ức chế bằng nhiều cách – theo đó cả thụ thể CD4 và vị trí gắn trên gp120 đều bị che phủ. Cả hai cách này đều được nghiên cứu. Nhóm thuốc ức chế gắn kết này có rất nhiều loại, bởi vậy không thể nói riêng về một loại thuốc.
Vào đầu thập kỷ 90 đã có một số nghiên cứu về phân tử CD4 hòa tan nhằm ngăn ngừa HIV gắn với tế bào CD4 (Daar 1990, Schooley 1990), nhưng chỉ đạt được kết quả in vitro mà không phải in vivo do thời gian bán hủy quá ngắn (vài phút) của phân tử CD4 hòa tan. Nhưng với sự tiến bộ trong hiểu biết về cơ chế HIV xâm nhập vào tế bào và cũng như sự thành công của loại thuốc ức chế xâm nhập đầu tiên T-20 thì quá trình phát triển các thuốc ức chế virus gắn kết đã được tiếp thêm động lực. Tuy vậy hầu hết các thuốc vẫn chưa đạt tiến bộ đáng kể, thường là có những vấn đề khó giải quyết về dược động học và đang trong giai đoạn tìm kiếm các bằng chứng về tác dụng của thuốc.
TNX-355 (trước đây là “Hu5A8”) là một kháng thể đơn dòng gắn với receptor CD4 và bởi thế ngăn ngừa HIV xâm nhập vào tế bào. Tuy nhiên cơ chế tác dụng của thuốc chưa được mô tả rõ. Ngược lại với các loại thuốc ức chế virus gắn kết khác, TNX-355 có vẻ không ngăn cản gp120 gắn vào CD4, mà tác động vào sự biến hình và gắn gp 120 vào CCR5 và CXCR4.
Thuốc đang được Tanox Biosytem (Houston, Texas) chế tạo. Nó chỉ được dùng đường truyền tĩnh mạch. Những dữ liệu ban đầu (Jacobsen 2004, Kuritzkes 2004) và kết quả 48 tuần của nghiên cứu thử nghiệm pha II đối chứng giả dược cho kết quả rất đáng khích lệ (Norris 2005). Ở nghiên cứu này, các bệnh nhân đã từng được điều trị rộng rãi ART sẽ được truyền TNX-355 mỗi 2 tuần trong năm theo 2 mức liều lượng (10 mg/kg hoặc 15 mg/kg) hoặc giả dược, cả hai nhóm đều được điều trị với công thức ART tối ưu. Sau 48 tuần, đã có sự giảm kéo dài tải lượng virus tới 1 log ở cả 2 nhánh của thử nghiệm.
Từ các kết quả đó TNX-355 có lẽ là thuốc mới thú vị nhất của y học HIV. Có tương quan ngược chiều giữa độ nhạy với TNX-355 và độ nhạy với CD4 hòa tan (Duensing 2006). Liệu chức năng của CD4 có bị ảnh hưởng hay không thì vẫn còn chưa rõ. Cho tới nay vẫn chưa thấy có ảnh hưởng có hại gì và vị trí gắn của TNX-355 trên CD4 là khác với vị trí gắn tự nhiên của CD4 với MHC lớp II. CD4 vẫn có thể thực hiện chức năng của nó kể cả khi TNX- 355 đã chiếm vị trí gắn với HIV. Ít nhất thì chúng ta cũng hy vọng như vậy.
BMS-488,043 là một thuốc ức chế virus gắn kết ra đời từ sớm của công ty BMS, thuốc này gắn đặc hiệu và có thể đảo nghịch với gp120 của HIV và nhờ đó ngăn cản HIV gắn với tế bào CD4. Khác với TNX-355, thuốc không gắn với thụ thể CD4. Vào đầu năm 2004, những kết quả đầu tiên trên bệnh nhân nhiễm HIV được công bố (Hanna 2004). Ở những bệnh nhân được dùng liều 800 mg hoặc 1800 mg hai lần mỗi ngày, tải lượng virus sau 7 ngày dùng đơn trị với cả 2 nhóm dùng thuốc giảm xuống lần lượt là 0.72 và 0.96 log. 15/24 bệnh nhân có tải lượng virus giảm xuống trên 1 log. Trong nghiên cứu này thấy thuốc dung nạp tốt. Tuy vậy vẫn còn gánh nặng do phải dùng nhiều viên thuốc mỗi ngày, điều này đòi hỏi phải cải tiến công thức bào chế. Ngoài ra, kháng thuốc có thể xuất hiện rất nhanh do vị trí gắn gp120 là một trong những vị trí biến thiên mạnh. Loại thuốc ức chế gắn kết này có thể hữu dụng để chế tạo thuốc diệt vi sinh (microbicide) (Kadow 2006).
