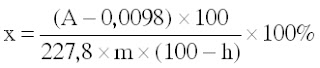3.1.3. Định tính, định lượng anthranoid trong dược liệu
3.1.3.1. Định tính hợp chất anthranoid trong dược liệu
a. Phản ứng Borntraeger
Nguyên tắc của phản ứng: Các hợp chất anthranoid khi tác dụng với kiềm (amoniac, natri hydroxyd hoặc kali hydroxyd) sẽ tạo các dẫn chất phenolat có màu đỏ sim tan trong nước.
* Định tính dạng tự do
· Chiết xuất
Lấy một lượng dược liệu thích hợp cho vào ống nghiệm lớn (10ml). Thêm 5ml nước cất. Đun trực tiếp với nguồn nhiệt cho đến sôi. Lọc dịch chiết còn nóng qua giấy lọc hoặc qua một lớp bông mỏng vào trong bình gạn dung tích 50ml. Làm nguội dịch lọc. Thêm 5ml ether (hoặc cloroform). Lắc nhẹ. Gạn bỏ lớp nước. Giữ lớp ether (hoặc cloroform) để làm phản ứng.
· Tiến hành phản ứng:
– Lấy 1ml dịch chiết ether (hoặc cloroform) cho vào ống nghiệm nhỏ. Thêm 1ml dung dịch amoniac 10%. Lắc nhẹ. Lớp nước sẽ có màu đỏ sim. Nếu lớp ether (hoặc cloroform) có màu vàng chứng tỏ trong dược liệu có chứa acid chrysophanic. Thêm tiếp tục từng giọt dung dịch NaOH 10%, lắc nhẹ. Lớp dung môi hữu cơ sẽ mất màu vàng, còn lớp nước sẽ đỏ thẫm hơn lúc ban đầu.
– Lấy 1ml dịch chiết ether (hoặc cloroform) cho vào ống nghiệm nhỏ. Thêm 1ml dung dịch NaOH 10%, lắc nhẹ. Lớp nước sẽ có màu đỏ sim.
– Lượng dược liệu thích hợp cho phản ứng:
Đại hoàng: 0,5g
Cốt khí củ, Thảo quyết minh, Hà thủ ô đỏ: 1g
* Định tính anthranoid toàn phần (dạng glycosid và dạng tự do)
Cho vào ống nghiệm lớn một lượng dược liệu thích hợp. Thêm 5ml dung dịch acid sulfuric 1N. Đun trực tiếp trên nguồn nhiệt đến sôi. Tiếp tục lọc và chiết như ở trên.
– Lấy 1ml dịch chiết ether (hoặc cloroform), thêm 1ml dung dịch amoniac. Lắc nhẹ. Lớp nước sẽ có màu đỏ sim. Nếu lớp ether có màu vàng thì tiếp tục nhỏ từng giọt dung dịch NaOH 10%. Lắc nhẹ. Lớp ether sẽ mất màu còn lớp nước thì màu sẽ đỏ đậm hơn.
– Lấy 1ml dịch chiết ether (hoặc cloroform) cho vào ống nghiệm nhỏ. Thêm 1ml dung dịch NaOH 10%. Lắc nhẹ. Lớp nước sẽ có màu đỏ sim.
Ghi chú:
Với dược liệu Hà thủ ô đỏ, muốn phản ứng lên rõ hơn có thể tiến hành như sau:
Lấy khoảng 0,5g bột dược liệu. Thêm 5ml dung dịch NaOH 2% trong ethanol. Đun trực tiếp với nguồn nhiệt cho đến sôi. Pha loãng với đồng lượng nước cất. Lọc nóng dung dịch vào trong bình gạn dung tích 50ml. Acid hóa đến phản ứng acid nhẹ. Thêm 5ml ether. Lắc mạnh. Tiến hành phản ứng định tính với dịch chiết ether như đã nêu ở trên.
b. Sắc ký lớp mỏng
– Dung dịch thử: Lấy 0,1g bột dược liệu (Đại hoàng) cho vào bình nón, thêm 30ml nước cất và 1ml acid hydrocloric đậm đặc (TT) đun cách thủy 15 phút. Để nguội, lọc, lắc dịch lọc với 25ml ether (hoặc cloroform). Gạn lấy lớp ether (hoặc cloroform), lọc qua natri sulfat khan. Bốc hơi dịch ether (hoặc cloroform) đến cắn. Hòa tan cắn bằng 1ml cloroform.
– Dung dịch đối chiếu: Hòa tan acid chrysophanic trong cloroform, nếu không có chất chuẩn đối chiếu acid chrysophanic, dùng bột Đại hoàng (mẫu chuẩn), tiến hành chiết như dung dịch thử.
– Bản mỏng Silicagel GF254 đã hoạt hóa ở 1050C trong 1 giờ.
– Dung môi khai triển: Ether dầu hỏa – ethyl acetat – acid formic (75 : 25 : 1).
– Cách tiến hành: Chấm riêng rẽ lên bản mỏng mỗi dung dịch trên. Sau khi triển khai sắc ký, quan sát bản mỏng dưới ánh sáng tử ngoại ở bước sóng 366nm. Sắc ký đồ của dung dịch thử phải có vết phát huỳnh quang màu vàng, có cùng giá trị Rf với acid chrysophanic trên sắc ký đồ của dung dịch đối chiếu. Các vết huỳnh quang vàng chuyển thành màu đỏ khi hơ bản mỏng trong hơi amoniac hoặc phun thuốc thử KOH 5%/EtOH. Nếu dùng dược liệu đối chiếu, trên sắc ký đồ của dung dịch thử phải có các vết cùng màu sắc và giá trị Rf với các vết trên sắc ký đồ của dung dịch đối chiếu.
c. Các phản ứng vi hóa
· Phản ứng vi hóa
Cắt một lát vi phẫu mỏng, không tẩy rửa, không nhuộm. Đặt lát cát vào trong hộp petri có chứa hơi amoniac. Sau một thời gian soi lát cắt dưới kính hiển vi. Các tổ chức có chứa các dẫn chất anthranoid sẽ có màu nâu đỏ.
· Vi thăng hoa
Trải bột dược liệu thành lớp mỏng trong một nắp chai bằng nhôm, đốt nhẹ trên đèn cồn để loại nước. Sau đó đậy lên nắp nhôm một miếng lam kính, bên trên có miếng bông đã thấm nước, tiếp tục đun nóng trong khoảng 5 – 10 phút. Lấy lam kính ra để nguội, soi kính hiển vi thấy tinh thể hình kim màu vàng. Sau khi nhỏ dung dịch natri hydroxyd lên lam kính, dung dịch sẽ có màu đỏ.
3.1.3.2. Định lượng hợp chất anthranoid
a. Định lượng anthranoid trong Đại hoàng theo Dược điển Việt Nam IV
Tiến hành:
Cân chính xác khoảng 0,1g bột dược liệu đã rây qua rây có kích thước mắt rây 0,180mm, cho vào bình nón có dung tích 250ml. Thêm 30ml nước cất và đun hồi lưu trong cách thủy 15 phút. Để nguội, thêm 50mg natri hydrocarbonat, lắc đều trong 2 phút. Ly tâm, lấy 10ml dịch trong cho vào một bình cầu dung tích 100ml, thêm vào đó 20ml dung dịch sắt (III) clorid 2% và đun hồi lưu trong cách thủy 20 phút. Sau đó thêm 1ml dung dịch acid hydrocloric đậm đặc và tiếp tục đun hồi lưu 20 phút nữa. Để nguội, chuyển tất cả hỗn hợp vào một bình gạn và chiết với ether ethylic ba lần, mỗi lần 15ml. Lọc lớp ether qua bông vào một bình định mức 100ml. Rửa phễu với ether và thêm ether tới vạch. Lấy chính xác 10ml dịch chiết ether cho vào cốc có mỏ dung tích 50ml và bốc hơi đến cắn.
Hòa tan cắn với 10ml dung dịch magnesi acetat 0,5% trong methanol, đo độ hấp thụ ở bước sóng 515nm với mẫu trắng là methanol.
Hàm lượng phần trăm dẫn chất hydroxyanthracen tính theo rhein, được tính theo công thức:
Theo quy định của Dược điển Việt Nam IV, dược liệu Đại hoàng phải chứa ít nhất 2,2% dẫn chất hydroxyanthracen tính theo rhein.
b.Định lượng anthranoid trong dược liệu bằng phương pháp đo quang
Nguyên tắc:
Dùng acid acetic để thủy phân các dạng anthraglycosid thành dạng aglycon. Chiết xuất bằng dung môi hữu cơ (ether hoặc cloroform). Tiến hành phản ứng Borntraeger với dịch chiết. Đo mật độ quang của dung dịch ở bước sóng 515nm.
Các bước tiến hành:
· Chiết xuất
Cân chính xác a gam bột dược liệu (0,050g nếu là Đại hoàng, 0,100g nếu là các dược liệu khác: Cốt khí củ, Thảo quyết minh, Hà thủ ô đỏ …). Cho dược liệu vào bình cầu hoặc bình nón dung tích 250ml có lắp ống sinh hàn hồi lưu. Thêm 7,5ml acid acetic băng. Đun sôi trong 15 phút trên bếp điện có lưới amiang. Sau khi để nguội thêm vào bình (qua ống sinh hàn ngược) 30ml cloroform. Đun sôi 15 phút trên nồi cách thủy. Làm nguội dịch chiết. Gạn hỗn hợp cloroform – acid qua phễu có giấy lọc vào bình gạn dung tích 100ml (giấy lọc gấp nếp nhỏ đến mức độ tối thiểu có thể). Bột trong bình cùng với giấy vừa lọc lại được đun hồi lưu tiếp tục với 20ml cloroform trong 10 phút. Gạn dịch chiết qua phễu có giấy lọc vào bình gạn trên. Rửa bình và giấy lọc với 10ml cloroform. Gộp các dịch chiết cloroform.
· Làm phản ứng màu
Cho từ từ vào bình gạn có chứa dịch chiết cloroform 15ml dung dịch NaOH 40%. Lắc nhẹ, (phản ứng tỏa nhiệt, nếu cần, làm lạnh bình gạn dưới vòi nước lạnh). Thêm vào bình gạn 25ml dung dịch NaOH 5% có chứa 2% amoniac. Lắc đều. Gạn lớp nước có màu đỏ vào bình định mức 100ml. Tiếp tục lắc lớp cloroform với dung dịch NaOH 5% có chứa 2% amoniac đến khi lớp nước không còn có màu. Thêm dung dịch NaOH 5% có chứa 2% amoniac vào bình định mức đến đủ 100ml. Rót dung dịch ra một cốc có mỏ dung tích 200ml rồi đặt lên nồi cách thủy sôi trong 20 phút. Để nguội rồi cho lại vào bình định mức. Thêm dung dịch NaOH 5% có chứa 2% amoniac cho đủ 100ml.
· Đo mật độ quang
Đo mật độ quang ở bước sóng 515nm, cốc đo dày 1cm với mẫu trắng là dung dịch NaOH 5% có 2% NH4OH.
· Thành lập đường chuẩn và phương trình hồi quy tuyến tính
– Pha dung dịch mẫu chuẩn
Nguyên tắc: Cân chính xác 0,0100g acid chrysophanic hòa tan hoàn toàn trong 10ml cloroform. Dung dịch này được làm phản ứng màu Borntraeger theo phương pháp của Auterhoff.
Cho từ từ 15ml NaOH 40%, rồi 25ml dung dịch NaOH 5% có 2% NH4OH vào dung dịch trên, lắc, gạn lớp nước màu đỏ vào một bình định mức có dung tích 100ml, rồi lại lắc tiếp với dung dịch NaOH 5% có 2% NH4OH đến khi không màu. Gạn dung dịch màu vào bình định mức trên, thêm dung dịch NaOH 5% có 2% NH4OH cho đủ 100ml. Dung dịch này là dung dịch mẹ (nồng độ 0,1% = 10.10-3%) dùng pha các mẫu có nồng độ khác nhau để đo mật độ quang học.
– Pha dung dịch đo quang
Từ dung dịch mẫu chuẩn 10.10-3% pha một thang nồng độ từ 0,5.10-3 đến 2,5.10-3%.
Lấy 5ml dung dịch 10.10-3% pha thành 100ml, được dung dịch có nồng độ 0,5.10-3%. Tương tự lấy 10ml, 15ml, 20ml và 25ml dung dịch 10.10-3% pha thành 100ml, được dung dịch có nồng độ tương ứng là 1,0.10-3%; 1,5.10-3%; 2,0.10-3% và 2,5.10-3%.
– Đo mật độ quang học của thang dung dịch acid chrysophanic chuẩn ở bước sóng 515nm.
Nồng độ | 0,5.10-3 | 1,0.10-3 | 1,5.10-3 | 2,0.10-3 | 2,5.10-3 |
Độ hấp thụ A | 0,125 | 0,232 | 0,353 | 0,465 | 0,578 |
Đường chuẩn biểu diễn mối tương quan giữa mật độ quang học với nồng độ.
Đường chuẩn định lượng anthranoid trong dược liệu theo acid chrysophanic
Từ mối tương quan giữa mật độ quang học với nồng độ là tuyến tính, xây dựng được phương trình hồi quy tuyến tính y = 227,8x + 0,0098 với r2 = 0,999872 hay r2 = 1 trong đó y là mật độ quang học (A) và x là nồng độ.
· Tính kết quả
Hàm lượng phần trăm dẫn chất hydroxyanthracen trong dược liệu tính theo acid chrysophanic, được tính theo công thức:
A: mật độ quang học của dung dịch màu
m: khối lượng dược liệu
h: hàm ẩm dược liệu
x: hàm lượng phần trăm dẫn chất anthraquinon trong dược liệu
Ghi chú:
Kết quả thu được từ phương pháp trên là hàm lượng anthranoid toàn phần, bao gồm dạng tự do, dạng glycosid, dạng oxy hóa và dạng khử. Nếu muốn định lượng riêng từng dạng thì cần chú ý:
– Nếu muốn định lượng dạng tự do, bỏ qua quá trình thủy phân với acid acetic.
– Nếu muốn định lượng dạng oxy hóa thì bỏ qua quá trình đun nóng 20 phút trước khi đo mật độ quang học.
– Hàm lượng anthranoid dạng khử được tính từ mật độ quang của hiệu số 2 lần đo trước và sau khi đun nóng.
– Nồng độ dạng glycosid là hiệu số giữa nồng độ phần trăm dạng anthranoid toàn phần và dạng tự do.