Mục lục
MỞ ĐẦU
Ribozym là các phân tử acid ribonucleic (RNA) có khả năng tác động như các enzym ngay cả khi vắng mặt hoàn toàn các protein. Chúng có hoạt tính xúc tác bẻ gẫy và /hoặc hình thành các liên kết cộng hóa trị với tính đặc hiệu và gia tăng tốc độ các phản ứng một cách phi thường. Khả năng của RNA với tư cách một chất xúc tác lần đầu tiên được phát hiện trong tự ghép nối intron nhóm I của Tetrahymena với bán phần RNA của RNase P. Tiếp sau sự phát hiện 2 enzym RNA này là sự xúc tác qua trung gian RNA liên quan tới sự tự ghép nối các intron nhóm II của nấm men, nấm, và ty thể thực vật (cũng như lục lạp); các RNA virusoid và viroid thực vật chuỗi đơn; virus viêm gan delta; và RNA vệ tinh từ ty thể Neurospora. Khá rõ ràng là cấu thành RNA tiểu đơn vị lớn của ribosome có chức năng như là một peptidyltransferase. Với chức năng tiềm tàng thực thi các ghép nối nhân nhỏ hơn (spicesomal smaller nuclear snRNA) như ribozym nó lại liên hợp với tiền RNA thông tin (pre-mRNA) để xúc tác cho sự ghép nối pre -RNA. Cũng rất giống với motif xúc tác RNA bổ sung, những vai trò mới của xúc tác qua trung gian RNA cũng được phát hiện càng nhiều khi đi sâu tìm hiểu hệ gen của các cơ thể khác nhau. Ribozym cũng có thể là một hợp chất tự nhiên hay được tổng hợp nhân tạo để nhắm vào các trình tự đặc hiệu cis– hoặc trans-. Phạm vi các hoạt động hóa sinh in vitro nhằm lựa chọn các protocol cũng chưa được phát triển. Các ribozym có thể thao tác một cách dễ dàng để tác động lên các cơ chất mới. Các RNA được thiết kế theo đơn đặt hàng có tiềm năng lớn với tư cách là các tác nhân trị liệu và đang trở thành một công cụ mạnh đối với các nhà sinh học phân tử. Các ribozym xúc tác đầu búa (hammerhead) và cặp tóc (hairpin) là đại diện cho các lựa chọn phổ thông áp dụng trong trị liệu được mô tả trên Hình 5.1.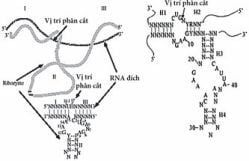
Hình 5.1. Các ribozym xúc tác hay được dùng nhất là dạng đầu búa và dạng cặp tóc. Trên hình vẽ là cấu trúc bậc hai của ribozym hình đầu búa. Trong đó: N = nucleotid bất kỳ, R = purin, Y = pyrimidin. Sơ đồ cấu trúc bậc 3 của ribozym hình đầu búa cũng được vẽ cạnh mô hình cấu trúc bậc 2 của nó. Các bộ phận (stem) tương ứng I, II và III ở cả 2 cấu trúc cũng được thể hiện. Trong ribozym hình đầu búa thì H =A, C hoặc U ở vị trí phân cắt. Trong ribozym hình cặp tóc thì H1, H2 là những vùng xoắn của cấu trúc RNA. (Theo Lisa Scherer và John J. Rossi. (2005) Cancer Gene Therapy. Human Press. Totowwa, New Jersey)
Sự gây nhiễu của RNA (RNA interference)
Sự gây nhiễu RNA (RNAi) là một cơ chế làm yên lặng gen được sáng tỏ một cách cội nguồn ở thực vật, cũng như là sự yên lặng gen sau phiên mã ở Caenorhabditis elegans và ruồi giấm Drosophila. Trong mô hình đương thời, con đường RNAi được hoạt hóa bởi một súng RNA sợi đôi (double-stranded RNA dsRNA), sau đó nó được xử lý thành những đoạn dsRNA ngắn từ 21 đến 22 nt được ám chỉ như là các RNA gây nhiễu nhỏ (small interfering RNA –siRNA) bởi một enzym tế bào có tên là Dicer (Hình 5.2A). Các siRNA sẽ hợp nhất thành phức hợp yên lặng cảm ứng RNA (RNA-induced silencing complex RISC), trong đó siRNA hoạt động với tư cách là kẻ dẫn đường nhận dạng mRNA để tiêu hủy. Trong các TB động vật có vú thì dsRNA dài hơn 30 nt sẽ làm bùng phát con đường interferon để hoạt hóa PKR và 2-5 – oligoadenylat synthase hơn là con đường RNAi. Tuy nhiên, các siRNA ngắn hơn được cài ngoại sinh vào các TB động vật có vú trong phiên mã nội sinh qua bước Dicer lại hoạt hóa trực tiếp sự thoái hóa mRNA tương đồng mà không cần khởi động đáp ứng interferon (Hình 5.2B).
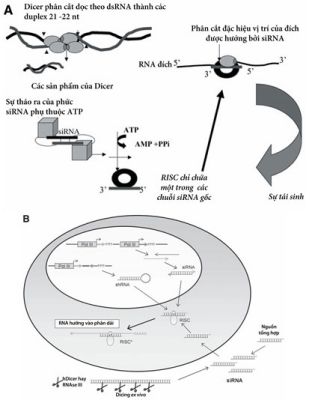
Hình 5.2. Cơ chế mRNA đích thoái hóa được hướng bởi siRNA trong các tế bào động vật có vú. (A) các dsRNA dài hơn 30bp được phân cắt bởi một thành viên họ RNase III tên là Dicer thành các siRNA 21-23-nt có 2 base 3 chồi ra. Các siRNA không bị tổn thương bởi phức helicase thì vẫn còn đặc tính và sợi antisense được cặp đôi bởi một phức hợp có tên là phức hợp yên lặng cảm ứng RNA (RNA-induced silencing complex RISC). RISC đảm trách phân cắt đặc hiệu vị trí RNA đích và tái chế. (B) siRNA đơn tổng hợp hoặc hỗn hợp của siRNA enzym gốc đi từ RNA đích có thể ghép nối một cách ngoại sinh. Có thể lựa chọn cách tạo ra SiRNA nội sinh bằng việc sử dụng hệ thống hộp kép trong đó siRNA được phiên mã như một vòng cặp tóc. Chưa rõ là vòng shRNA đã được xử lý như thế nào. (Theo Lisa Scherer và John J. Rossi. (2005) Cancer Gene Therapy. Human Press. Totowwa, New Jersey).
ỨNG DỤNG CỦA RIBOZYM
Các ribozym được ứng dụng như các tác nhân kháng virus, dùng để điều trị ung thư và các rối loạn di truyền và cũng là công cụ để làm sáng tỏ các con đường và phê chuẩn đích. Khởi đầu sử dụng ribozym là nhằm vào kháng virus, chủ yếu là điều trị virus gây thiếu hụt miễn dịch trên người (HIV). Các virus mà có thể tác động thông qua sản phẩm trung gian RNA hệ gen trong chu kỳ tái bản của chúng như HIV, virus gây viêm gan B, C đó là những đích hấp dẫn bởi vì các mẫu đơn ribozym có thể nhắm tới RNA hệ gen virus và cả các mRNA. Ribozym cũng được sử dụng rộng rãi đối với các gen tế bào đích bao hàm cả những gen biểu hiện một cách lầm lạc trong ung thư.
Đích ribozym đầu tiên là bản sao tổng hợp bcr-abl được kiến tạo từ nhiễm sắc thể Philadelphia liên quan tới bệnh bạch cầu dòng tuỷ mạn tính. Đặc trưng của nhiễm sắc thể này là bằng sự chuyển vị (translation) đã biểu hiện được protein tổng hợp bcr- abl tải nạp. Trong trường hợp này, ribozym được thiết kế để nhắm vào mRNA tổng hợp một cách đặc hiệu chứ không phải là nhắm vào bcr hay abl bình thường để ngăn chặn chức năng của gen gây ung thư bcr-abl. Khi đột biến ở codon 12 trong c-H-ras từ GGU thành GUU thì tạo nên một vị trí cho sự phân cắt qua trung gian ribozym đầu búa. Một ribozym biểu hiện nội sinh nhắm vào đích này đã có hiệu ứng ngăn ngừa sự hình thành tiêu điểm (focus formation) với khoảng 50% tế bào NIH3T3 đã được thâm nhiễm với gen ras hoạt hóa. Trái lại, các tế bào biểu hiện ribozym tương tự này nhưng lại thâm nhiễm với ras hoạt hóa trong đó có sự thay đổi codon ở vị trí 61 thay vì vị trí 12 thì không ngăn ngừa được sự hình thành tiêu điểm. Các ribozym nhắm vào HER- 2/neu được biểu hiện quá mức trong ung thư vú đã làm giảm đáng kể sự tạo u của các tế bào này trên chuột.
Hơn nữa, để nhắm trực tiếp vào các gen gây ung thư, các ribozym cũng được áp dụng một cách gián tiếp hơn với tư cách là các trị liệu kháng ung thư. Chẳng hạn như các riobozyme nhắm vào các gen kháng đa thuốc 1 (multiple drug resistance gene 1) hoặc fos mRNA trong các dòng tế bào ung thư đã tạo được các TB nhạy cảm hơn với các tác nhân hóa trị liệu. Mặt khác, ribozym nhắm vào bcl-2 đã làm bùng phát apoptosis trong các TB ung thư vùng miệng.
Các yếu tố đòi hỏi cho sự di căn cũng là đích hấp dẫn cho ribozym. Các ribozym nhắm mục tiêu chống lại CAPL/mts, metalloprotein gian bào (matrix), pleiotrophin và VLA-6 integrin đều làm giảm tiềm năng di căn của các TB khối u cần lưu tâm. Sự tạo mạch cũng là đích quan trọng cho gen trị liệu ung thư và quá trình này đã được ngăn chặn ở chuột bởi ribozym đích vào protein gắn yếu tố tăng trưởng nguyên bào sợi và pleiotrophin.
Các trị liệu với cơ sở ribozym đã được test ở động vật nhằm ức chế các rối loạn tăng sinh khác như tái hẹp động mạch vành. Antitelomerase RNA ribozym cũng được test để áp dụng trong gen trị liệu ung thư. Dĩ nhiên việc sử dụng ribozym như các tác nhân trị liệu cần có sự thay đổi phù hợp với từng loại ung thư.
Sự chuyển giao
Bất kỳ dạng ribozym nào định lựa chọn thì cũng phải đưa được vào các TB đích. Có 2 cơ chế chung về việc đưa các phân tử RNA xúc tác vào trong các TB – đó là chuyển giao ngoại sinh các ribozym hình thành trước (preformed ribozym) và biểu hiện nội sinh từ một đơn vị phiên mã. Ribozym hình thành trước có thể được chuyển vào trong các TB nhờ các phương thức: liposome, điện xung (electroporation) hoặc vi tiêm.
Rất nhiều phương pháp lý thú trong tổng hợp hóa học RNA và các dạng cải biến của RNA đã được thực hiện trong vài năm qua. Các phân tử có tính ổn định lâu dài trong huyết thanh hoặc trong các môi trường nội bào đã được tổng hợp. Một số ribozym với bộ khung cải biến vẫn duy trì được tính đặc hiệu vị trí và những đặc tính xúc tác của các RNA chưa cải biến, và một số lại làm tăng đặc tính xúc tác vì thế chúng trở thành các ứng cử viên cho sự chuyển giao ex vivo. Các ribozym cải biến hóa học thể hiện khả năng chuyển giao không cần capsul hóa mà vẫn vào được tế bào.
Biểu hiện nội bào ổn định các ribozym hoạt hóa phiên mã có thể thực hiện được nhờ chuyển giao qua trung gian vec tơ virus. Hiện nay, các vec tơ retrovirus thường hay được sử dụng nhất đối với tế bào nuôi cấy, các TB sơ cấp (gốc) và các TB động vật chuyển gen. Các vec tơ retrovirus có lợi thế là hợp nhất ổn định vào trong hệ gen TB chủ đang phân chia và tất nhiên là khi vắng mặt bất kỳ gen virus nào được biểu hiện cũng làm giảm ngẫu nhiên đáp ứng miễn dịch ở động vật. Hơn nữa, các retrovirus có thể tạo nên các dạng giả một cách dễ dàng với nhiều protein vỏ để nới rộng hoặc hạn chế tính hướng tế bào chủ vì thế mà tăng thêm mức độ đích TB cho sự chuyển gen ribozym. Các vec tơ adenovirus có thể được tạo ra ở các độ chuẩn cao và tải nạp rất hiệu quả nhưng nó lại không hợp nhất vào hệ gen vật chủ; vậy là sự biểu hiện của gen chuyển chỉ là tức thời trong các TB đang phân chia tích cực. Các hệ thống chuyển giao virus khác là virus adeno liên hợp, virus alpha và lentivirus. Virus adeno liên hợp được hấp dẫn bởi vì nó là virus nhỏ, không gây bệnh và có thể hợp nhất một cách ổn định vào trong hệ gen vật chủ. Với hệ virus alpha, khi sử dụng virus Semliki Forest tái tổ hợp đã cho hiệu ứng tải nạp cao đối với các TB động vật có vú biểu hiện ribozym tế bào chất.
Phương tiện vận chuyển khác cho sự chuyển giao ex vovo gen ribozym là cationic lipid. Vì có nhiều công thức lipid nên tốt nhất là chọn các lipid cho hiệu ứng cao nhất đối với sự chuyển gen mà độc tính lại ít nhất.
ĐỘNG VẬT CHUYỂN GEN BIỂU HIỆN RIBOZYM
Việc trị liệu và các nghiên cứu xác nhận đích chắc phải được thử nghiệm trên động vật. Các ribozym đã được sử dụng trong chuột chuyển gen nhằm kiến tạo các mô hình bệnh như đái tháo đường bằng việc điều hòa xuống một cách chọn lọc hexokinase mRNA trong các tiểu đảo của tụy. Trong trường hợp này, sự biểu hiện ribozym được kiểm soát bởi promoter insulin vì thế nó chỉ biểu hiện ở các tế bào của tụy. Sự chuyển giao ribozym bằng retrovirus để kháng lại neuregulin 1 ở phôi gà cũng ngang bằng với kiểu hình (phenotype) gây tổn hại phôi với tư cách là một gen knockout. Khi định vị được sự chuyển giao bằng retrovirus với một ribozym tương tự thì sau đó có thể phân tích được một cách kỹ lưỡng con đường hóa sinh của neuregulin. Dùng ribozym cảm ứng nhiệt kháng fushi tarzu ở ruồi giấm sẽ làm gián đoạn đúng lúc sự tiến triển chức năng này ở phôi ruồi giấm.
SỬA CHỮA RNA QUA TRUNG GIAN RIBOZYM
Một áp dụng trị liệu mới của các ribozym là khai thác hoạt tính ghép nối trans của ribozym Tetrahymena. Ribozym được sử dụng để sửa chữa mRNA khiếm khuyết một trình tự chức năng gây bởi sự ghép nối trans trên các RNA này. Những ribozym này được thiết kế để liên kết và phân cắt các RNA 5’ đích của đột biến không mong muốn. Vì ribozym trong trường hợp này là một intron nên nó được công nghệ hóa để thực hiện việc chỉnh sửa trình tự RNA với tư cách là 3exon. Tiếp sau sự phân cắt RNA đích đột biến là ribozym xúc tác gắn trình tự hoang dã vào bản sao đã phân cắt. Đây là minh chứng đầu tiên về sự hiệu chỉnh của bản sao Lax Z đột biến ở vi khuẩn và sau đó là hiệu chỉnh thông tin tế bào liềm trong các tế bào dòng hồng cầu.
SỰ TIẾN HÓA CỦA RIBOZYM
Việc phát hiện ra ribozym đã làm bùng phát tranh cãi mới về giả thuyết “thế giới RNA” (RNA world), theo đó thì tất cả các quá trình sinh hóa đều được thực hiện bởi enzym có nền tảng RNA. Kể từ đó, sự tiến hóa RNA bắt buộc phải đi từ in vitro để tiến gần tới những enzym RNA có khả năng thực hiện đa dạng rộng các phản ứng hoá sinh như hình thành liên kết carbon -carbon và liên kết peptide. Tiến hóa RNA in vitro được sử dụng để kiến tạo các ribozym phân cắt RNA với các domain nhỏ hơn, các ribozym phân cắt DNA và các motif xúc tác mới. Ngay cả enzym DNA phân cắt RNA cũng được tạo ra thông qua tiến hóa (những thay đổi) in vitro. Những enzym tiến hóa (evolved) này là ví dụ điển hình về sức mạnh của tiến hóa in vitro.
Cũng có lý để kết luận rằng việc đạt được các tương tác cơ chất – enzym hiệu ứng và chức năng ribozym trong môi trường gian bào không phải là một công việc dễ dàng và các chiến lược mới cho sự biểu hiện và định vị ribozym trong các môi trường gian bào là một nhu cầu đòi hỏi để cho phép sử dụng một cách phổ biến các ribozym như các tác nhân trị liệu.
NHỮNG CÂN NHẮC KHÁC
Mặc dầu tính đặc hiệu về sự cặp đôi base đã tạo dựng được đích chọn lọc, làm tối thiểu hóa các độc tính tiềm ẩn nói chung. Nhưng vấn đề độc tính thì vẫn phải làm test một cách nghiêm khắc bởi vì khi các ribozym làm mất sự cặp đôi đối với một cơ chất không phải là đích có thể sẽ tạo ra hiệu ứng ức chế antisense không mong muốn. Vì bất kỳ một trình tự ribozym nào cũng có các tương tác cặp đôi base tiềm tàng khác nhau, vì thế việc tích lũy các số liệu từ các thí nghiệm về ribozym khác nhau là cần thiết cho việc đánh giá sự tiềm ẩn này một cách nghiêm khắc. Một số tiềm ẩn về độc tính là sự tương tác không đặc hiệu của ribozym với các protein của tế bào hay việc phát sinh sự tập trung cao tại gian bào các sản phẩm phân cắt và hiệu ứng ức chế sự chuyển hóa tế bào do các cải biến hóa học khi tiền tổng hợp ribozym.
Một trong số các lợi thế tiềm tàng của ribozym so với các RNA antisense là hoạt tính xúc tác của chúng mà về lý thuyết có thể dẫn đến làm bất hoạt nhiều cơ chất đích. Tuy nhiên, cũng cần phải chứng minh liệu hoạt tính xúc tác này có xảy ra ở gian bào không? Có lẽ là sự luân chuyển cơ chất qua trung gian ribozym gian bào đã tạo thuận lợi cho sự phân cắt qua trung gian ribozym đầu búa. Các thí nghiệm được thiết kế để phát hiện các protein tạo thuận lợi cho sự luân chuyển ribozym gian bào hiện nay mới chỉ được thực hiện ở một vài phòng thí nghiệm. Việc làm giầu sự liên hợp ribozym – protein cùng với nâng cao hoạt tính xúc tác cũng đã được thăm dò trong các chiến lược khám phá in vitro. Sau chót là việc thiết kế mẫu và tổng hợp hóa học các ribozym nhằm tạo khả năng luân chuyển xúc tác cao bởi các base đặc hiệu và những cải biến bộ khung cũng cần được thực hiện.
DỰ KIẾN TRONG TƯƠNG LAI
Khái niệm ribozym có thể là các tác nhân trị liệu mới chỉ xuất hiện trong vòng mấy năm gần đây. Tuy nhiên, vấn đề lớn cần quan tâm là việc triển khai sử dụng trong lâm sàng các ribozym trong tương lai gần nhất. Tại thời điểm này thì vẫn còn vội vã khi kết luận rằng ribozym sẽ có một vị trí trong danh mục các tác nhân trị liệu trong y học hiện đại. Còn nhiều vấn đề cần phải tìm hiểu về sự dịch chuyển của RNA bên trong TB cũng như các yếu tố TB có thể gây trở ngại hay tạo thuận lợi cho việc sử dụng ribozym. Những vấn đề này không đơn giản chút nào, nhưng không vì thế mà làm hạn chế các nghiên cứu ứng dụng ribozym. Khi các kỹ thuật trong sinh học TB càng tinh tế hơn thì câu trả lời cho các vấn đề này cũng sắp tới gần.
Việc biến nạp các trình tự ribozym từ các phân tử phân cắt (và kết nối) dạng cis tự nhiên thành các tác nhân phân cắt (và kết nối) dạng trans đặc hiệu đích đã khích động rất lớn tiềm năng ứng dụng của chúng. Các ribozym nhắm đích các gen virus hiện nay đang được đánh giá về lâm sàng, các ribozym nhắm đích các gen TB sẽ được chuyển vào các động vật chuyển gen và việc sử dụng ribozym đang được mở rộng sang các lĩnh vực nghiên cứu tiến hóa RNA, sửa chữa mRNA và phát hiện các gen.
Để ribozym trở thành các tác nhân trị liệu thực sự thì những cản trở đầu tiên phải được vượt qua. Những cản trở phải kể đến là việc chuyển giao một cách hiệu quả (theo tỷ số %) tới một quần thể tế bào, biểu hiện hiệu quả ribozym từ một vec tơ hay tập trung ribozym ở gian bào, colocalization (trong hiển vi huỳnh quang, colocalization là muốn nhắc đến các phương pháp phân tích số liệu khác nhau để xác định đặc trưng về độ trùng lặp giữa 2 mẫu đánh dấu huỳnh quang khác nhau, mỗi mẫu có một bước sóng phát xạ khác nhau để xác định xem các đích TB khác nhau có định vị trên cùng một vùng hay là rất gần với một vùng khác) của ribozym với đích, tính đặc hiệu của ribozym đối với các mRNA mong muốn và việc nâng cao vòng luân chuyển cơ chất qua trung gian ribozym. Nhờ những hiểu biết về cấu trúc bậc 3 và 4 của RNA ngày càng được nâng cao mà RNA lại là đích ngắm chuẩn trong việc giải quyết các vấn đề thuộc tính đặc hiệu. Đồng thời, sự am hiểu về định vị vật lý của các RNA trong TB cũng như đường đi của nó khi dịch chuyển từ nhân tới tế bào chất chắc chắn sẽ giúp cho colocalization của các ribozym và đích. Những cải biến ribozym (2ribose) với các tác nhân khác như các nhóm methyl, alkyl, fluoro và amino đã làm tăng rất đáng kể tính ổn định đối với các nuclease. Tương tự như vậy, các ribozym DNA-RNA chimeric cũng làm tăng thêm tính ổn định. Hiệu lực của việc chuyển giao tới TB bằng các vec tơ virus hay liposom cũng đang được nâng cao không ngừng. Những phân tử này phải duy trì được tiềm năng xúc tác của chúng, đồng thời phải tiến đến được vị trí dễ bị ảnh hưởng trên cơ chất và phải tác động một cách hiệu quả, vững chắc đối với các phân tử đích, điều đó rất hữu ích đối với các công cụ di truyền thay thế cũng như với các tác nhân trị liệu. Những tiến bộ lớn đạt được trong tất cả các lĩnh vực này sẽ cho phép sử dụng rộng rãi các tác nhân đặc hiệu cao để điều hòa xuống sự biểu hiện của các RNA đích.
RNA gây nhiễu
Chúng ta sẽ tập trung vào một số lợi thế hiện tại của việc sử dụng các công nghệ dựa trên cơ sở RNAi trong các hệ động vật có vú, chủ yếu nhắm vào việc áp dụng trong nghiên cứu ung thư. Sau cùng chúng ta sẽ so sánh các cách tiếp cận với việc sử dụng siRNA và ribozym trong điều hòa xuống các đích mRNA đặc hiệu.
siRNA là các thực thể chức năng được tạo ra do sự phân cắt các dsRNA dài hơn bởi enzym Dicer. Thông thường nhất là các duplex với chiều dài 21-22 nt, có 2 base 3 nhô ra. Cả siRNA và short hairpin RNA (shRNA) đều có thể được tổng hợp hóa học và đã đưa vào một cách ngoại sinh hay biểu hiện một cách nội sinh từ một promoter (Hình 5.2B). In vitro, các Kit phiên mã để tạo ra các siRNA đã là sản phẩm thương mại vì người ta đã tổng hợp được bằng phương pháp hóa học.
Về vấn đề biểu hiện, đã có 2 mẫu thiết kế thành công về siRNA. Mẫu thứ nhất bắt chước sản phẩm Dicer tự nhiên, cấu tạo gồm 2 RNA 21-nt, đặc biệt có 2 phần nhô ra ở mỗi đầu 3. Phần nhô ra kinh điển chỉ bao gồm 2 uridin, còn phần nhô ra này lại có thể đi từ trình tự đích đã nhắm trước. Các dòng siRNA dài hơn có chiều dài tới 29-nt có thể được sử dụng mà không có đáp ứng interferon trong các tế bào động vật có vú. Mẫu thiết kế thứ hai muốn nhắc đến là shRNA , cấu trúc gồm bản sao đơn của cả các trình tự sense và antisense được nối với nhau bằng một vòng ghim. Với vòng ghim chừng 4-nt là đã có một phần siRNA hiệu ứng, nhưng với các vòng dài hơn tới 9 nt thì sẽ chắc chắn hơn.
Vì các promoter pol III hiệu ứng một cách đặc hiệu trong phiên mã siRNA và shRNA nên có thể suy luận được sự thoái hóa mRNA đặc hiệu đích.
Promoter U6 + 1 có những đặc tính làm cho nó thích hợp một cách đặc biệt cho việc biểu hiện siRNA. U6 +1 là một promoter bên ngoài (external) tạo được sự biểu hiện cao ở nhiều dạng TB. Sự phiên mã được bắt đầu từ guanosin khởi đầu đặc hiệu và kết thúc hành trình với 4 hoặc nhiều hơn trình tự uridin trong bản sao, việc cắt bỏ 3’ poly u lồi ra được nhận dạng bởi cỗ máy RISC. Cuối cùng, các promoter tương đối nhỏ thì đưa được vào nhiều bộ khung vec tơ rất dễ dàng. Ngoài ra, promoter pol III cũng đã được thăm dò, còn promoter pol II thì vẫn chưa được nghiên cứu nhiều.
Các vec tơ plasmid chuẩn cũng có thể được sử dụng cho việc biểu hiện nhanh một cách nội sinh các siRNA. Cả episome và các vec tơ retrovirus đều đã có được sự biểu hiện ổn định. Một số công trình có sử dụng vec tơ lentivirus để biểu hiện dài hạn các siRNA. Các vec tơ lentivirus đã được đóng gói có lợi thế là chúng có thể biến nạp được cả các TB đang phân chia cũng như các TB không phân chia.
RNAi và các ứng dụng trong ung thư
siRNA hiện nay đang được thăm dò với tư cách là một công cụ điều hòa xuống các sản phẩm của nhiễm sắc thể Philadelphia – kết quả của chuyển vị giữa gen BCR trên NST số 22 và ABL trên NST số 9 không có quan hệ với nhau, tạo nên một gen ung thư hợp nhất (oncogenic fusion gene). Kết quả cho thấy: gen và bản sao của BCR/ABL có mặt ở hầu hết các bệnh nhân mắc bệnh bạch cầu dạng tủy mạn tính (chronic myeloid leukemia CML), cũng như 30% ở người lớn mắc bệnh bạch cầu tăng lympho huyết cấp tính (acute lymphoblastic leukemia), những người này đáp ứng rất thấp với các trị liệu thông thường. Có 2 cách giải thích được xác định dựa trên các điểm dừng khác nhau trong BCR: M-BCR và m -BCR tạo nên các protein ung thư M -BCR/ABL và m -BCR/ABL với khối lượng phân tử lần lượt là 210 kDa và 19 kDa. Protein lai ghép này có hoạt tính kinase cao hơn chất tương đồng ABL của TB, có thể nghĩ rằng nó là một bộ phận của dòng thác hiệu ứng dẫn đến phát triển ung thư và ức chế apoptosis.
Willda và cộng sự đã sử dụng dòng TB của người bị bệnh bạch cầu dòng tủy mạn tính (chronic myelogenous leukrmia cell line) biểu hiện M -BCR/ABL mRNA để test khả năng của siRNA tổng hợp đối với việc điều hòa xuống đặc hiệu tương ứng với tín hiệu và protein, làm tăng sự nhạy cảm của TB đối với apoptosis. Khi thâm chuyển tức thời siRNA nhắm vào việc kháng lại vùng cầu nối chung M -BCR/ABL đã làm giảm xuống đặc hiệu các mức p210 nhưng không ảnh hưởng tới protein ABL hoặc vimentin nội sinh. Một siRNA đối chứng mà bắt cặp không đúng ở cả 2 chuỗi tương ứng với khoảng 17-18 base chuỗi antisense thì không có hiệu ứng. Điều quan trọng hơn là khi giảm cảm ứng siRNA của bản sao ung thư lại tạo được các hiệu ứng sinh lý học mong muốn như các TB trở nên nhạy cảm hơn với apoptosis. Với các oligonucleotid sense hay antisense riêng rẽ M -BCR/ABL siRNA đột biến hay siRNA kháng lại các đích tương đồng trong hỗn hợp m -BCR/ABL (không thấy trong những TB này) thì lại không làm tăng apoptosis. M -BCR/ABL siRNA cũng cảm ứng apoptosis với các mức tương tự như các tác nhân hóa trị liệu STI 571 trong 72 giờ, mặc dầu động học có thấp hơn. Người ta không quan sát thấy hiệu ứng cộng khi sử dụng cả STI 571 và siRNA; tuy nhiên, chỉ thấy có một nồng độ STRI571 được test là gây cảm ứng apoptosis gần mức tối đa. Sơ bộ về đáp ứng liều thuận nghịch đối với M
-BCR/ABL siRNA và STI 571 thì thấy có sự hợp tác với nhau. Tuy nhiên, những kết quả này cũng đã cho các bằng chứng về siRNA có thể làm giảm một cách đặc hiệu với nhiều mức độ bản sao ung thư và làm đảo ngược phần nào các đặc tính tăng trưởng ung thư trong hệ mô hình dòng tế bào.
Scherr và cộng sự xác nhận có sự giảm đặc biệt M -BCR/ABL trong các tế bào K562 nhờ điện xung với siRNA cùng loại và chỉ rõ rằng các mức c -bcr và c -abl nội sinh đều không có sự biến đổi (đối với GAPDH tế bào). Hơn nữa, khi thâm chuyển siRNA vào các tế bào TonB 210.1 của chuột nhà có chứa M -BCR/ABL có thể cảm ứng được đã làm giảm cả mức mRNA và protein sau cảm ứng; khả năng sống của TB đồng thời cũng bị suy giảm gần như với STI 571 trong các thí nghiệm trước đó. Các tác giả cũng đã test để xem M -BCR/ABL siRNA liệu có làm giảm tăng sinh cảm ứng cytokin hay không cũng như sự tăng sinh đem đến từ ber /abl vào trong các tế bào TonB. Nếu thêm interleukin 3 (IL-3) thì sẽ làm đảo ngược ức chế tăng sinh cảm ứng bởi cả STI 751 và siRNA, mặc dầu mức độ giảm BCR/ABL mRNA cũng giống như với các tế bào được xử lý với siRNA có hoặc không có IL-3. Như vậy, M-BCR/ABL siRNA đã làm giảm ức chế tăng trưởng phụ thuộc arb /abl nhưng không phụ thuộc cytokin.
Kết quả này được chú ý một cách đặc biệt dưới ánh sáng của các thực nghiệm sau này ở tế bào sơ cấp. Khi điện xung M -BCR/ABL siRNA vào trong tế bào PBMC hoặc CD34+ thuần khiết lấy từ 6 bệnh nhân bị bệnh bạch cầu dòng tủy mạn tính cùng với siRNA đã làm giảm bản sao ung thư tới 50-79%. Tuy nhiên, không thấy có sự ức chế hoặc giảm tăng trưởng hình thành quần thể khi TB sơ cấp đã thâm nhiễm với siRNA, sau khi đã được tăng trưởng trong môi trường lỏng hoặc bán lỏng có bổ sung cytokin trong các thử nghiệm về tăng sinh hay hình thành quần thể. Trái lại, trong xử lý đối chứng với STI 751 thì lại có hiệu ứng. Không thấy có sự giảm tăng trưởng phụ thuộc M -BCR/ABL siRNA ở các dòng TB sơ cấp, điều đó chứng tỏ độ pha loãng siRNA đã vượt ngưỡng trong thời gian thực nghiệm, hoặc do ảnh hưởng của cytokin được cho thêm vào trong nuôi cấy TB, điều này cũng phảng phất như các kết quả thu được trong các tế bào TonB. Tuy nhiên, trong các tế bào TonB thì IL-3 lại cho hiệu ứng cả với siRNA cũng như STI 751. STI 751 cũng bị ức chế trong các thử nghiệm về hình thành quần thể. Tình trạng này sẽ được sáng tỏ như lặp lại các thử nghiệm với biểu hiện ổn định của M -BCR-ABL siRNA từ bộ khung lentivirus. Tất cả những thử nghiệm này đã vẽ được bức tranh thể hiện siRNA có thể là một phương pháp hiệu lực làm giảm bản sao ung thư đặc hiệu. Tuy nhiên, các kết quả đạt được trong các TB nuôi cấy có thể sẽ không phải như vậy.
Tương tự như vậy, siRNA cũng chưa được test với đích là gen hỗn hợp ALM1/MTG8 do sự chuyển vị giữa nhiễm sắc thể 21 và nhiễm sắc thể 8, thường xảy ra ở mức 10-15% trong các bệnh nhân AML de novo.
Hỗn hợp ALM1/MTG8 đã làm chuyển đổi chức năng bình thường của AML1 với tư cách một chất hoạt hóa phiên mã điều hòa sự tạo máu thành chất kiềm chế (repressor) trội trans chủ yếu, dẫn các TB tới trạng thái biến nạp ung thư.
Để hiểu rõ hơn vai trò của AML/MTG8 trong sự hình thành bệnh bạch cầu, người ta đã sử dụng siRNA trong nghiên cứu về hiệu ứng kiềm chế protein ung thư ở các dòng TB gây bệnh bạch cầu ở người Kasumi – 1 và SKNO-1. Các tác giả đã thiết kế một số siRNA đích đặc hiệu mRNA của hỗn hợp AML/MTG8, tương tự như các thí nghiệm với BCR/ABL. 16 giờ sau khi biến nạp với các tế bào Kasumi -1, các thử nghiệm đã chỉ rõ: ở nồng độ 200-nm AML/MTG8 siRNA đã làm giảm một cách đặc hiệu mRNA ung thư liên quan tới AML1 nội sinh, khi so sánh với AML1/MTG8 siRNA đột biến và không thích hợp. Những kết quả tương tự cũng quan sát thấy trên cả các tế bào SKNO-1 và Kasumi -1 khi thực nghiệm với Real – time reverse transcriptase polymerase chain reaction đã được chuẩn hóa đối với GAPDH tế bào. Sự kiềm chế các bản sao ung thư kéo dài trong 5 ngày, song song với việc giảm đáng kể protein tương ứng ít nhất 4 ngày sau thâm chuyển; AML tế bào thì không bị tác động.
Tiếp theo là các AML/MTG8 siRNA cũng được sử dụng để xác định hiệu ứng thứ cấp cảm ứng điều hòa xuống các protein. Các thí nghiệm trước đó cũng đã đề cập tới các protein sinh ung thư với việc can thiệp điều hòa xuống cảm ứng cytokin bình thường của CD11 và receptor yếu tố kích thích quần thể đại thực bào (macrophage colony-stimulating factor M-CSF) bằng việc suy luận sự biệt hóa bạch cầu đơn nhân trong các tế bào Kasumi -1 và SKNO-1; AML1/MTG8 gắn một cách đặc hiệu vào yếu tố tăng trưởng biến nạp SMAD3 (transforming growth factor (TGF-b) activated transcription factor SMAD3) tiềm tàng khả năng tạo ra một khối biệt hóa dòng tủy qua trung gian TGF –b/vitamin D3. Vả lại, protein hỗn hợp gắn vào C /EBP- lại rất cần thiết cho sự tăng trưởng bạch cầu hạt. Các tác giả đã sử dụng AML1/MTG8 siRNA để kết nối sự điều hòa xuống của protein hướng tới sự tái hiện các đặc tính biệt hóa. AML1/MTG8 siRNA đơn lẻ chỉ làm tăng nhẹ số tế bào Kasumi -1 dương tính với CD11b (CD11b- positive Kasumi-1 Cells). Tuy nhiên, khi AML1/MTG8 siRNA kết hợp với xử lý bằng TGF-b1 và vitamin D3 thì các tế bào Kasumi -1 lại biểu hiện làm giảm sự tăng trưởng dòng; tăng số lượng tế bào dương tính marker biệt hóa dòng tủy CD11b từ mức tối đa là 20% (TFG-b1-b/ vitamin D-B3-b đơn lẻ) lên mức 40-60%; tăng đáng kể sự biểu hiện receptor M -CSF bề mặt; và tăng 60 lần mức C
/EBP- tế bào (vượt 15 lần so với AML1/MTG8 siRNA đơn lẻ). Những kết quả này càng khẳng định hơn vai trò của AML1/MTG8 siRNA trong kiềm chế cảm ứng bắt nguồn từ cytokin đối với sự biệt hóa dòng tủy, duy trì trạng thái tế bào blast của bạch cầu và rõ ràng là có thể ứng dụng được các siRNA trong việc phân tích gen.
Ví dụ sau chót là RNAi nhắm vào các sản phẩm của chuyển vị, nó sản sinh ra một protein ung thư hỗn hợp EWS/Fli-1, phát hiện thấy ở 85% ung thư Ewing và ở các TB khối u biểu bì thần kinh (neuroectodermal) gốc. Có 2 sự trùng lặp đích bất đối siRNA ở khe nối hỗn hợp được biểu hiện từ promoter U6+1 trong TC135 dòng TB ung thư Ewing. EWS/Fli-1 siRNA làm giảm một cách đặc biệt mRNA hỗn hợp liên quan tới -actin tế bào. Tuy nhiên, vị trí II siRNA chứa 17 base tương đồng với Fli
-1 cũng làm giảm phần nào Fli -1 mRNA nội sinh. Mặc dầu vậy, không xảy ra sự đảo nghịch; vị trí I siRNA chứa 17 base tương đồng với EWS tế bào chỉ điều hòa xuống một cách đặc hiệu với bản sao ung thư. Những kết quả này đã làm nổi bật tầm quan trọng của việc theo dõi sự kiềm chế chéo tiềm tàng của các bản sao nội sinh khi sử dụng RNAi. Các tế bào TC135 được đồng chuyển cùng với EWS/Fli-1 và vec tơ biểu hiện eGFP sẽ làm giảm vận tốc tăng trưởng trong nuôi cấy 3 tuần. Hơn nữa, sự biểu hiện c -Myc được hoạt hóa bởi protein EWS/Fli-1 cũng giảm xuống khi được xử lý với siRNA.
Tóm lại, các siRNA rất hiệu lực trong việc làm giảm mức protein ung thư hỗn hợp như M -BCR/ABL, AML/MTG8 và EWS/Fli-1. Những kết quả này đã chứng minh khả năng sử dụng siRNA như một tác nhân trị liệu các bệnh ung thư và có thể kết hợp cùng với việc trị liệu bằng thuốc. Thành công của việc tiếp cận này sẽ còn phụ thuộc một phần vào các siRNA có thể làm trung gian cả trong việc làm giảm bớt các bản sao ung thư đích cũng như thay đổi sinh lý sự điều hòa xuống theo ý muốn trong các tế bào ung thư sơ cấp.
So sánh siRNA và ribozym
siRNA hiện rõ như một công cụ mạnh đánh gục (knock down) các bản sao mRNA một cách đặc hiệu. Vì vậy, một câu hỏi cần được đặt ra là khi nào thì ta chọn công nghệ siRNA hay là công nghệ khác dựa trên cơ sở acid nucleic? Để đáp ứng phần nào vấn đề này, ở phần kết của chương này sẽ bình luận một cách ngắn gọn: so sánh việc sử dụng ribozym và siRNA cũng như các lợi thế tiềm tàng của mỗi cách tiếp cận.
Hiện nay chúng ta đều hiểu rõ rằng sự dung nạp đối với những cải biến, nới rộng đời sống bán phần cũng như hiệu quả trong các ứng dụng nhất thời của ribozym cao hơn siRNA. Chắc rằng cần phải có các thí nghiệm xa hơn xác định mức độ và dạng của các cải biến hóa học mà siRNA có thể dung nạp được.
Các dẫn liệu đã được xuất bản chỉ rõ các chức năng chủ chốt và có thể là độc quyền của siRNA ở trong tế bào chất; do vậy siRNA không đích các intron và chỉ có một vị trí đích siRNA ở một isoform mRNA đặc hiệu mới là khớp nối exon -exon duy nhất. Tuy nhiên vẫn còn nghi ngờ rằng liệu vị trí này có kháng lại được sự thoái hóa của siRNA hay không?. Cũng vì lẽ ấy, ribozym có thể được sử dụng nhờ có lợi thế cao với việc phân giải mRNA trước khi nó tới được tế bào chất. Chẳng hạn như trong các giai đoạn sớm của sự sao chép HIV trong tế bào thì xu hướng kiểm soát dễ dàng hơn vì các chất ức chế acid nucleic với tư cách là các mRNA mã hóa cho các protein điều hòa ít dư thừa hơn so với các gen cấu trúc muộn. Cũng có thể là việc ức chế xuất khẩu những RNA sớm, mã hóa cho các protein điều hòa sớm Tat và Rev đã ngăn chặn khởi đầu sự tái bản virus hoạt hóa. Chẳng hạn như ribozym anti -HIV hướng vào các thành phần của nhân đã ức chế thành công sự tái bản HIV. Việc phát hiện một vị trí đích đặc hiệu trong mRNA vẫn có thể là mơ hồ đối với thiết kế của cả siRNA và ribozym. Tuy nhiên, nếu sự lựa chọn các vị trí đích bị giới hạn thì ribozym có thể không được sử dụng nếu vị trí này không bao hàm cả vị trí phân cắt cặp ba thích ứng. Có một nhận xét là nếu vị trí đích đặc hiệu lại đổi hướng với siRNA thì hiện nay chưa có sự lựa chọn nào khác cho việc cải tiến sự phân cắt đối với vị trí đó. Có nhiều sự lựa chọn colocalization để nâng cao tính nhạy cảm của ribozym bằng cách định hướng các hợp phần đặc biệt của TB và colocalization định hướng trình tự tới đích. Tuy nhiên, ribozym lại có sự chắp thêm các trình tự đích không liền kề vì thế mà nó có thể việc colocalize đích và ribozym đồng thời lại tạo thuận lợi cho việc thay đổi cấu trúc làm cho vị trí đích trở thành hữu ích. Yêu cầu về kích thước của siRNA chính là để phòng ngừa việc sử dụng các trình tự chắp thêm, mặc dầu vậy vẫn có ngoại lệ và có thể nhiều quá trình sinh hóa của siRNA và microRNA liên quan đã được hiểu rõ. Việc xác định các đặc trưng của RNA lai ghép liên quan tới cả microRNA và siRNA cũng đã được tiến hành.
Việc sử dụng siRNA vẫn tiếp tục được mở rộng, đặc biệt khi các cơ chế hóa sinh đã được tường tận hơn. Tuy nhiên, không hy vọng RNAi có thể được sử dụng thay thế cho ribozym, aptamer cũng như các cách tiếp cận toàn diện khác.
Các siRNA với tư cách là một công cụ bổ sung kết hợp cùng với các trị liệu khác trên cơ sở acid nucleic thì sẽ tạo được hiệu ứng trị liệu cao hơn.
