Phát sinh sau phần lớn các ung thư hay gặp bên trong cơ thể con người; chiếm khoảng 10% tỷ lệ tử vong liên quan đến ung thư ở Hoa Kỳ; tỷ lệ mắc tăng đột ngột trên 50 tuổi, gần như ngang nhau ở nam và nữ.
Trong năm 2012, 143,460 ca mắc, 51,690 ca tử vong.
Nguyên nhân và các yếu tố nguy cơ
Phần lớn ung thư đại tràng có nguồn gốc từ các polyp tuyến. Các bậc di truyền từ polyp đến loạn sản thành ung thư tại chỗ, ung thư thâm nhiễm đã được xác định, bao gồm đột biến điểm trong gen tiền ung thư K-ras, giảm quá trình methyl của DNA dẫn đến tăng cường sự biểu lộ gen, mất allen tại gen APC (gen ức chế khối u), mất allen tại gen DCC (loại bỏ ung thư đại tràng) trên nhiễm sắc thể số 18, và sự đột biến và mất p53 trên nhiễm sắc thể số 17. Bệnh ung thư đại tràng di truyền không polyp có nguồn gốc từ đột biến các gen sửa chữa lỗi chuyển đoạn ADN , gen hMSH2 trên nhiễm sắc thể số 2 và gen hMLH1 trên nhiễm sắc thể số 3. Những đột biến dẫn tới ung thư đại tràng và các ung thư khác. Chẩn đoán đòi hỏi ba hoặc nhiều hơn người thân cận bị ung thư đại tràng, một trong số đó là người thân mức đầu tiên; một hoặc nhiều trường hợp được chuẩn đoán trước tuổi 50; và liên quan ít nhất với 2 thế hệ. Yếu tố môi trường cũng góp phần; tăng nổi trội ở những nước đang phát triển, khu vực thành thị, các nhóm kinh tế xã hội; tăng nguy cơ ở bệnh nhân tăng cholesterol trong máu; bệnh động mạch vành; nguy cơ tương ứng với ít chất xơ, chế độ ăn có chất béo động vật cao, mặc dù ảnh hưởng trực tiếp của chế độ ăn vẫn còn chưa sáng tỏ; sự giảm nguy cơ khi bổ sung calci bữa ăn trong thời gian dài và uống aspirin hàng ngày. Tăng nguy cơ ở những người thân mức đầu tiên của bệnh nhân; liên quan mật thiết với tăng tỷ lệ của ung thư; và bệnh nhân có tiền sử ung thư vú hoặc sinh dục, hội chứng đa polyp gia đình, tiền sử >10 năm bệnh viêm loét đại tràng hoặc viêm đại tràng Crohn, tiền sử >15 năm mở thông đại tràng sigma – tử cung. Các khối u ở bệnh nhân với tiền sử gia đình bị bệnh ác tính thường được khu trú ở đại tràng bên phải và xuất hiện trước tuổi 50; tỷ lệ cao ở bệnh nhân nhiễm vi khuẩn Streptococcus bovis.
Bệnh học
Hầu hết là ung thư biểm mô tuyến; 75% được khu trú ở đại tràng góc lách (trừ khi phối hợp với đa polyp hoặc các hội chứng ung thư đại tràng di truyền); có thể giống polyp , không cuống, giống nấm hoặc co thắt; dưới nhóm và mức độ biệt hóa đều không liên quan tới diễn biến bệnh. Phân độ xâm nhập (phân loại Dukes) là tiên lượng đơn thuần tốt nhất (Hình).
Các khối u trực tràng-sigma có thể sớm lan tới phổi vì hệ thống dẫn lưu tĩnh mạch cạnh sống của vùng này. Các dấu hiệu khác tiên lượng nghèo nàn: lượng kháng nguyên ung thư biểu mô phôi trước phẫu thuật (CEA) >5 ng/mL (>5 μg/L), hình ảnh mô học biệt hóa nghèo nàn, thủng ruột, thâm nhiễm tĩnh mạch, dính vào cơ quan xung quanh, lệch bội, mất đoạn đặc biệt trong nhiễm sắc thể số 5, 7,18, và đột biến gen tiền ung thư ras. 15% có khuyết thiếu gen sữa chữa DNA.
Đặc diểm lâm sàng
Triệu chứng thường gặp của ung thư đại tràng bên trái là chảy máu trực tràng, thay đổi các thói quen đại tiện (phân dẹt nhỏ, táo bón. tiêu chảy mạn tính, khó đại tiện), và đau lưng hoặc bụng; Ung thư đại tràng lên và manh tràng thường xuất hiện các triệu chứng thiếu máu, máu ẩn trong phân, hoặc sụt cân; các biến chứng khác: thủng ruột, lỗ rò, xoắn ruột, thoát vị bẹn; kết quả cận lâm sàng: thiếu máu trong 50% các thương tổn ở bên phải.
Chẩn đoán
Chẩn đoán sớm được bổ trợ bằng sàng lọc ở người không triệu chứng với xét nghiệm máu trong phân (xem dưới đây); > 50% các ung thư đại tràng trong tầm 60 cm của dụng cụ nội soi đại tràng sigma tự do ; thụt bayrit cản quang – khí sẽ chẩn đoán ~85% các ung thư đại tràng mà không trong tầm của dụng cụ nội soi đại tràng sigma, nội soi đại tràng nhạy và đặc hiệu nhất, cho phép sinh thiết khối u và gỡ bỏ đồng bộ các polyp ( điều này ngăn chặn chuyển thành khối u), nhưng tốn kém hơn. X quang và nội soi ảo không được thể hiện là phương pháp chẩn đoán tốt hơn nội soi đại tràng.
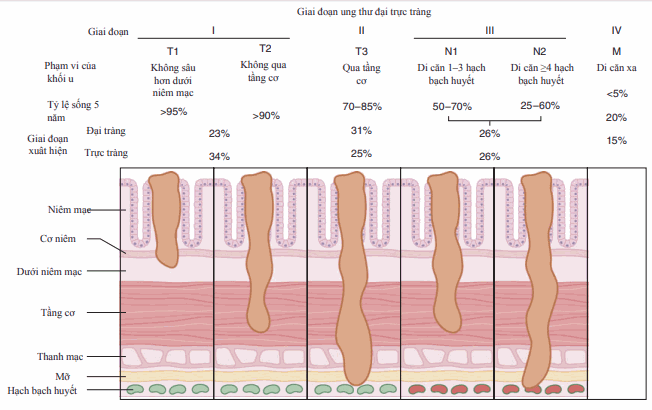
Hình. Các giai đoạn và tiên lượng bệnh nhân ung thư đại trực tràng.
Điều trị ung thư đại trực tràng
Bệnh khu trú: Phẫu thuật cắt bỏ phần đại tràng chứa khối u; Đánh giá trước phẫu thuật để bổ trợ tiên lượng và phương pháp phẫu thuật bao gồm nội soi toàn bộ đại tràng, phim x quang ngực, xét nghiệm sinh hóa gan, nồng độ CEA huyết thanh, và có thể CT bụng. Có thể cắt bỏ các phần di căn gan bị cô lập ở những trường hợp chọn lọc. Điều trị xạ trị hỗ trợ vùng khung chậu (có hoặc không đi kèm hóa trị 5FU) giảm tỷ lệ tái phát tại chỗ của K trực tràng (không ảnh hưởng rõ rệt trên tỷ lệ sống thêm); xạ trị không có lợi ích trên các khối u trực tràng; điều trị xạ trị trước phẫu thuật có thể cải thiện phần có thể cắt bỏ và kiểm soát tại chỗ trong bệnh nhân K trực tràng. Trong K trực tràng cắt bỏ toàn bộ phần giữa trực tràng hiệu quả hơn cắt bỏ phần trước- sau. Hỗ trợ hóa trị (5FU/leucovorin với oxaliplatin, hoặc FOLFOXvới bevacizumab, hoặc 5FU/leucovorin với irinotecan, hoặc FOLFIRI) giảm tỷ lệ tái phát và cải thiện sống thêm trong giai đoạn C (III); lợi ích sống thêm do điều trị hóa trị không rõ ràng trong các khối u giai đoạn B (II); xét nghiệm định kỳ nồng độ CEA hữu ích trong theo dõi điều trị và đánh giá tái phát. Theo dõi sau cắt bỏ chữa trị: Xét nghiệm chức năng gan hằng năm, công thức máu toàn phần, giám sát x quang hoặc nội soi đại tràng sau 1 năm nếu bình thường, 3 năm 1 lần với sàng lọc thường quy; nếu các polyp được phát hiện,lặp lại 1 năm 1 lần sau khi cắt bỏ. Khối u tiến triển (không thể cắt bỏ tại chỗ hoặc di căn): Hóa trị hệ thống (5FU/leucovorin kết hợp oxaliplatin với bevaci-zumab), irinotecan thường được sử dụng trong điều trị hỗ trợ; Kháng thể với receptor EGF (cetuximab, panitumumab) thể hiện tăng cường hiệu quả của hóa trị; xạ trị trong động mạch [floxuridine (FUDR)] và/ hoặc xạ trị có thể giảm bớt các triệu chứng từ di căn gan.
Phòng chống
Sàng lọc máu trong phân thường quy (Hemoccult II, ColonCare, Hemosure) có thể thuận lợi cho việc phát hiện sớm K đại tràng; tuy nhiên, độ nhạy chỉ ~50% cho K biểu mô; độ dặc hiệu cho khối u hoặc polyp ~25-40%. Dương tính giả: tiêu hóa thịt đỏ, sắt, aspirin, xuât huyết tiêu hóa cao.
Âm tính giả: ăn uống vitamin C, chảy máu dai dẳng. Thăm khám tay trực tràng hằng năm và xét nghiệm máu trong phân được đề nghị cho những bệnh nhân trên tuôi 40, sàng lọc bằng nội soi đại tràng sigma linh 3 năm 1 lần sau 50 tuổi, sớm hơn ở những bệnh nhân có yếu tố nguy cơ cao; đánh giá cẩn thận ở những bệnh nhân có xét nghiêm máu trong phân dương tính (nội soi đại tràng sigma linh động và thụt baryt cản quang – khí hoặc nội soi đại tràng đơn độc) cho thấy nhiều polyp trong 20-40% và K biểu mô ~5%; sàng lọc bệnh nhân không triệu chứng cho phép phát hiện sớm ung thư đại tràng (i.e., giai đoạn Duckes sớm hơn ) và đạt được tỷ lệ có thể phẫu thuật lớn hơn; giảm tử vong nói chung do ung thư dạ dày chỉ quan sát được sau 13 năm theo dõi. Đánh giá sàng lọc tốt hơn cho người thân của bệnh nhân thường gồm thụt baryt cản quang – khí hoặc nội soi đại tràng sau tuổi 40. NSAIDs và ức chế cyclooxygenase 2 thể hiện sự ức chế phát triển của khối u và gây sự hồi quy khối u ở những nhóm có nguy cơ cao, nhưng không được khuyến cáo ở những bệnh nhân có nguy cơ trung bình tại thời điểm này.
Ung thư hậu môn
Chiếm khoảng 1-2% ung thư đại tràng, 6230 trường hợp và 780 chết trong năm 2012; thường đi kèm với kích thích ruột mãn tính, mụn cóc sinh dục, nứt/ rò xung quanh hậu môn, trĩ mãn, bạch sản, chấn thương trong sinh hoạt tình dục. Phụ nữ thường mắc nhiều hơn nam giới. Đàn ông đồng tính có nguy cơ cao. HPV là nguyên nhân gây ra. Các triệu chứng gồm chảy máu, đau, khối quanh hậu môn. Điều trị xạ trị kết hợp với hóa trị (5FU và mitomycin) dẫn tới đá ứng hoàn toàn trong 80% khi tổn thương tiên phát < 3 cm. Cắt bỏ phúc mạc với nội soi dạ dày lâu dài được dành riêng cho những người có nhiều tổn thương lớn hoặc tái phát sau hóa trị liệu.
